Những ngày qua, dư luận đặc biệt chú ý đến thông tin về thuốc ung thư Pembroria do Nga sản xuất. Nhiều người kỳ vọng đây là bước tiến mới trong điều trị ung thư.
Chưa thể đánh giá chất lượng
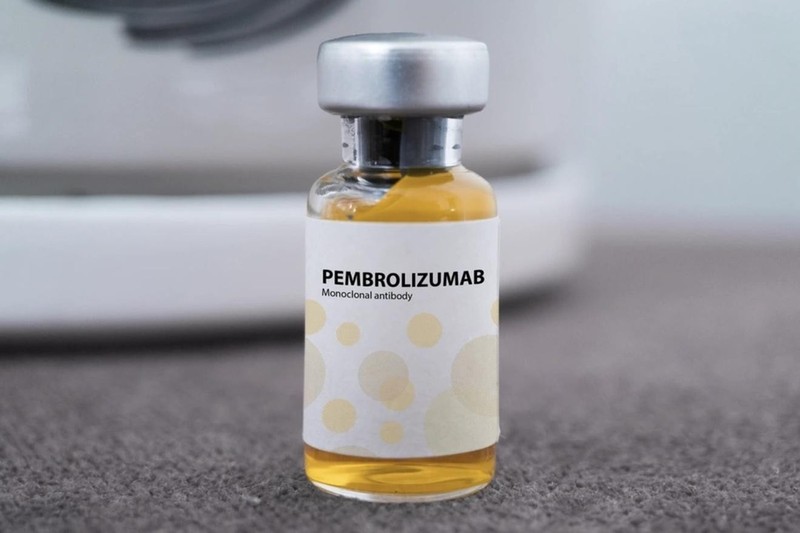
Tuy nhiên, điều quan trọng cần khẳng định là pembrolizumab không phải thuốc mới xuất hiện trên thị trường. Đây là thuốc gốc của Mỹ đã được phê duyệt nhiều năm, có hệ thống bằng chứng lâm sàng đồ sộ.
Sản phẩm do Nga sản xuất là phiên bản tương tự sinh học, nghĩa là có cùng bản chất hoạt chất và cơ chế nhưng sản xuất bởi Công ty Limited Liability "PK-137" (Nga) và một cơ sở tại Các Tiểu vương quốc Ả Rập Thống nhất đăng ký.
Vì thế, người bệnh không nên hiểu nhầm đây là thuốc “đời mới”, mà cần chú ý tuân thủ hướng dẫn theo đúng hồ sơ kỹ thuật của thuốc gốc và khuyến cáo của bác sĩ điều trị.
Theo tiêu chuẩn quốc tế, thuốc tương tự sinh học buộc phải chứng minh hiệu quả và độ an toàn tương đương với thuốc gốc, đặc biệt là theo dõi tính sinh miễn dịch để đảm bảo thuốc không gây phản ứng bất lợi hoặc hoạt tính miễn dịch vượt ngoài dự đoán.
Trong quyết định cấp phép, Bộ Y tế yêu cầu thuốc này phải cập nhật tiến độ nghiên cứu tính sinh miễn dịch pha III định kỳ ba tháng kể từ ngày cấp số đăng ký. Điều này phản ánh dữ liệu hiện tại còn thiếu và Pembroria vẫn trong giai đoạn tiếp tục hoàn thiện bằng chứng.
Thuốc dự kiến năm 2026 mới có mặt trên thị trường Việt Nam. Bởi vậy, mọi nhận định về chất lượng thuốc này đều chưa có cơ sở.
Chỉ định rộng nhưng hiệu quả bỏ ngỏ
Theo hồ sơ kỹ thuật của thuốc do cơ sở tại Các Tiểu vương quốc Ả Rập Thống nhất đăng ký, đưa ra thì các chỉ định của Pembroria tương tự thuốc gốc pembrolizumab, vốn được sử dụng rộng rãi trong nhiều phác đồ ung thư: Điều trị u hắc tố, ung thư phổi không tế bào nhỏ, ung thư đầu cổ, u lympho Hodgkin kinh điển, ung thư đường tiết niệu, thực quản, đại trực tràng, cổ tử cung, thận, nội mạc tử cung, ung thư vú bộ ba âm tính, ung thư dạ dày – chỗ nối dạ dày thực quản và ung thư đường mật.
Phần lớn các chỉ định yêu cầu xét nghiệm dấu ấn sinh học như PD-L1 hoặc tình trạng MSI-H/dMMR để xác định bệnh nhân phù hợp, bảo đảm dùng thuốc đúng đối tượng có lợi nhất.
Việc điều trị phải được thực hiện tại các cơ sở chuyên khoa với đội ngũ bác sĩ ung bướu có kinh nghiệm, bởi cơ chế kích hoạt hệ miễn dịch của pembrolizumab không đơn giản như hóa trị.
Hiệu quả của pembrolizumab gốc đã được chứng minh qua nhiều thử nghiệm lâm sàng lớn, giúp cải thiện đáng kể thời gian sống thêm cho nhiều nhóm bệnh nhân ung thư.
Tuy nhiên, hiệu quả tương đương của Pembroria đến đâu chỉ có thể khẳng định khi dữ liệu nghiên cứu tính sinh miễn dịch pha III của nhà sản xuất được hoàn thiện và công bố đầy đủ.
Những nguy cơ cần chú ý
Với bản chất là liệu pháp miễn dịch, pembrolizumab và các thuốc tương tự sinh học như Pembroria có thể gây ra những phản ứng bất lợi qua trung gian miễn dịch. Khi hệ miễn dịch bị “kích hoạt”, cơ thể có thể tự tấn công vào mô lành và gây viêm phổi, viêm đại tràng, viêm gan, viêm thận, viêm tuyến giáp, viêm tuyến yên.
Hồ sơ kỹ thuật của thuốc cũng báo cáo một số phản ứng bất lợi ở bệnh nhân được điều trị bằng pembrolizumab như nhiễm khuẩn đường tiết niệu, viêm phổi, giảm tiểu cầu, bạch cầu, đau cơ xương, đau khớp …
Một số trường hợp hiếm gặp nhưng nghiêm trọng như hội chứng Stevens–Johnson, hoại tử thượng bì nhiễm độc, viêm cơ tim hay viêm não được ghi nhận trong các báo cáo quốc tế về pembrolizumab.
Những biến cố này đòi hỏi phát hiện sớm và xử trí kịp thời. Phần lớn trường hợp độ 2 trở lên cần dùng corticosteroid liều cao và tạm ngừng thuốc; các phản ứng độ 3, 4 có thể phải dừng thuốc vĩnh viễn. Người bệnh cần tuân thủ theo dõi nghiêm ngặt suốt quá trình điều trị và cả sau khi ngừng thuốc, bởi phản ứng miễn dịch có thể xuất hiện muộn vài tuần.
Chỉ định sử dụng thuốc tuyệt đối không được tự ý hay điều trị ngoài hệ thống bệnh viện. Toàn bộ quá trình phải được giám sát bởi bác sĩ được đào tạo về liệu pháp miễn dịch, có khả năng nhận biết sớm diễn biến bất thường.
Việc một thuốc tương tự sinh học như Pembroria được phát triển và dự kiến đưa vào Việt Nam mở ra thêm lựa chọn cho người bệnh trong tương lai, khi tăng nguồn cung và giá rẻ hơn thuốc gốc. Tuy vậy, điều quan trọng nhất vẫn là minh bạch dữ liệu lâm sàng, tuân thủ tiêu chuẩn quốc tế về thuốc tương tự sinh học và chứng minh hiệu quả – an toàn tương đương thuốc gốc.
Khi những điều kiện này được đáp ứng đầy đủ, Pembroria mới có thể trở thành lựa chọn an toàn và đáng tin cậy cho bệnh nhân ung thư tại Việt Nam. Việc hiểu đúng về thuốc gốc và thuốc tương tự sinh học cũng giúp người bệnh yên tâm phối hợp điều trị và tránh các kỳ vọng không chính xác.

Cục Quản lý Dược: Thuốc ung thư Pembrori của Nga không phải thuốc mới