Liên doanh dược phẩm Việt đầu tiên mua lại vốn góp của nước ngoài
Công ty TNHH Liên doanh Stellapharm, Tổng Giám đốc – Dược sĩ Ông Văn Dũng, (số 40, đại lộ Tự Do, khu công nghiệp Việt Nam – Singapore, phường An Phú, thị xã Thuận An, tỉnh Bình Dương) được thành lập vào năm 2000 (tiền thân là Công ty TNHH Liên doanh STADA – Việt Nam), hiện là doanh nghiệp sản xuất dược trong lĩnh vực xuất khẩu dược phẩm tại Việt Nam, đặc biệt là thị trường các nước Châu Âu (SRA).
Chất lượng sản phẩm của Stella đã được công nhận trên toàn cầu thông qua sự đánh giá và công nhận của các nhà chức trách dược trên thế giới như Cơ quan Quản lý thuốc Châu Âu (EMA), Cục Dược phẩm và Thiết bị Y tế Nhật Bản (PMDA), Cục quản lý Thực phẩm và Dược phẩm Đài Loan (Taiwan FDA), Tổ chức Y tế Thế giới (WHO) và các Cơ quan khác. Các sản phẩm của Stella hiện có bán tại hơn 50 quốc gia trên toàn thế giới.
Xây dựng nền tảng từ năm 1995 từ Công ty TNHH Dược phẩm Khương Duy - một trong những Công ty dược tư nhân đầu tiên tại Việt Nam được thành lập vào năm 1995, hoạt động trong lĩnh vực phân phối các sản phẩm nhập khẩu. Đến năm 1999, ban lãnh đạo của Khương Duy đã nhận ra rằng sẽ rất khó phát triển hoạt động kinh doanh nếu không có những sản phẩm riêng của công ty. Tại thời điểm đó, Công ty nhận thấy việc sản xuất thuốc generics là một bước tiến trong bảo vệ sức khỏe con người.
Công ty đã quyết định thành lập Nhà máy sản xuất dược phẩm M.S.T vào đầu năm 2000 tại TP. Hồ Chí Minh, dưới tên gọi là Công ty TNHH Dược phẩm M.S.T.
Công ty TNHH Thương mại Dược phẩm M.S.T là nhà máy sản xuất dược phẩm tư nhân đầu tiên tại Việt Nam kể từ sau năm 1975. Nhà máy M.S.T được xây dựng và bắt đầu hoạt động vào đầu năm 2001, sản xuất các loại thuốc viên, thuốc nước và thuốc dùng ngoài với công suất thiết kế đạt 40 triệu đơn vị /tháng. M.S.T cũng trở thành Công ty sản xuất dược phẩm tư nhân đầu tiên được Bộ Y tế Việt Nam công nhận đạt tiêu chuẩn ASEAN GMP.
Để đầu tư mở rộng hoạt động kinh doanh phù hợp với tốc độ tăng trưởng của thị trường trong nước, M.S.T đã quyết định thành lập Liên doanh 50-50 với Tập đoàn STADA Arzneimittel, Đức. Đây là Công ty Dược phẩm Liên doanh đầu tiên tại thời điểm đó. Liên doanh chính thức đi vào hoạt động từ tháng 1 năm 2003 với tên Công ty Liên doanh TNHH STADA – Việt Nam.
 |
| Công ty TNHH Liên doanh Stellapharm (số 40, đại lộ Tự Do, khu công nghiệp Việt Nam – Singapore, phường An Phú, thị xã Thuận An, tỉnh Bình Dương) - Ảnh: website công ty |
Vào năm 2002, HIV/AIDS trở thành một vấn đề sức khỏe lớn ở Việt Nam. Công ty Liên doanh TNHH STADA – Việt Nam đã quyết định ra mắt thuốc ARV dưới tên Lamzidivir, là sản phẩm thuốc điều trị ARV đầu tiên được sản xuất trong nước. Sản phẩm này đã thu hút rất nhiều sự quan tâm từ các cấp chính quyền, các tổ chức sức khỏe cộng đồng…cho đến các phương tiện truyền thông trong nước và quốc tế vào thời điểm đó. Liên doanh STADA – Việt Nam được công nhận là tiên phong trong lĩnh vực sản xuất dược phẩm trong nước.
Liên doanh STADA – Việt Nam sau đó đã quyết định xây dựng nhà máy hiện đại thứ hai tuân thủ theo các hướng dẫn của Cơ quan Quản lý Dược phẩm Châu Âu (EMA). Đồng thời, một Đơn vị Nghiên cứu & Phát triển mới cũng được thành lập. Nhà máy mới không chỉ nhằm phục vụ thị trường trong nước mà còn giúp Liên doanh STADA-VN vươn ra thị trường nước ngoài, kể cả thị trường Châu Âu.
Một tháng sau khi được Bộ Y tế Việt Nam đánh giá và công nhận đạt tiêu chuẩn WHO-GMP vào tháng 12 năm 2007, Đơn vị thanh tra thuộc Cơ quan Quản lý Dược phẩm Châu Âu (EMA) đã chính thức công nhận Nhà máy đạt tiêu chuẩn Thực hành tốt sản xuất thuốc theo tiêu chuẩn Châu Âu EU-GMP vào tháng 2 năm 2008.
Liên doanh STADA – Việt Nam trở thành nhà máy sản xuất dược phẩm đầu tiên tại Việt Nam được Cơ quan Quản lý Dược phẩm Châu Âu (EMA) chứng nhận đạt tiêu chuẩn EU-GMP, đồng thời là Doanh nghiệp Dược đầu tiên được phép nhập khẩu vào Đức.
Đồng thời, Đơn vị R&D của STADA – Việt Nam cũng trở thành một trong những đơn vị Nghiên cứu & Phát triển dược phẩm trong nước lớn mạnh nhất, tạo nền tảng cho Liên doanh STADA – Việt Nam mở rộng thị trường xuất khẩu.
Từ năm 2008 đến nay, nhiều Cơ quan quản lý Dược phẩm các nước SRA đã tiến hành thanh tra Nhà máy của STADA – Việt Nam (WHO PQ, TFDA, PMDA), tất cả các đợt thanh tra đều được đánh giá tốt đẹp.
 |
| Những hình ảnh mới nhất ghi nhận từ bên trong nhà máy sản xuất thuốc đặc trị COVID-19 Stellapharm ở Bình Dương - Ảnh: Tiền Phong |
Năm 2011: Nhà máy II của STADA – Việt Nam đạt được WHO – GMP bởi Tổ chức Y tế Thế giới (WHO Geneva).
Năm 2014, nhà máy II ở Bình Dương, Việt Nam được chứng nhận đạt tiêu chuẩn GMP Nhật, một trong những quốc gia có ngành Dược phẩm phát triển nhất thế giới.
Năm 2017: Sản lượng sản xuất của đơn vị này đạt 2,8 tỷ đơn vị/ năm; Doanh thu hợp nhất của Liên doanh vượt mức 100 triệu USD; Thị trường xuất khẩu của Công ty đã vượt hơn 50 quốc gia và vùng lãnh thổ. Công ty TNHH Liên doanh STADA – Việt Nam trở thành nhà xuất khẩu sản phẩm dược lớn nhất Việt Nam.
Tuy nhiên, vì là một liên doanh 50-50, STADA- Việt Nam bắt đầu bị ảnh hưởng bởi một số hạn chế nhất định trong chiến lược tăng trưởng. Vào giữa năm 2017, Khương Duy và M.S.T quyết định trở thành cổ đông lớn của Liên doanh bằng cách mua lại phần vốn góp từ STADA Pharmaceutical (Asia) Limited, một công ty con Tập đoàn STADA Arzneimittel, Đức. Các cuộc đàm phán đã được tích cực theo đuổi và cơ bản đã thống nhất vào cuối năm 2017.
Trong năm 2018, Công ty này đã ký Thỏa thuận nhượng quyền với Hetero và Gilead cho phép Công ty sản xuất sản phẩm điều trị viêm gan C. Đây là một dòng sản phẩm đột phá cho Công ty trong việc tăng cường danh mục sản phẩm và cam kết của chúng tôi với bệnh nhân về chăm sóc sức khỏe.
Công ty dự kiến đưa ra thị trường sản phẩm Lesovir, một sản phẩm kết hợp liều cố định (Viêm gan C) tại Việt Nam vào Quý 1 năm 2020 nhằm giúp đỡ bệnh nhân có thu nhập thấp và trung bình có thể tiếp cận phương pháp điều trị này.
Theo lộ trình mua lại phần vốn góp, Công ty TNHH Liên doanh STADA – Việt Nam đã tiến hành đổi tên thành Công ty TNHH Liên doanh Stellapharm vào ngày 16 tháng 08 năm 2019.
Vào ngày 20 tháng 12 năm 2019, Công ty TNHH Dược phẩm M.S.T và Auxilto Healthcare International Private Limited thành công trong việc mua lại 42% và 8% phần vốn góp của STADA Pharmaceutical (Asia) Limited trong Công ty TNHH Liên Doanh Stellapharm. Với sự kiện này, Công ty TNHH Dược phẩm M.S.T nắm giữ 92% phần vốn góp và Auxilto Healthcare International Private Limited nắm giữ 8% phần vốn góp của Liên doanh, xác lập một kỷ lục mới, trở thành Công ty dược phẩm đầu tiên tại Việt Nam mua lại thành công phần vốn góp của đối tác nước ngoài. Liên doanh tăng trưởng đều đặn với tỷ lệ 8% hàng năm.
Năm 2020, Công ty TNHH Liên doanh Stellapharm cùng nhà thầu Liên doanh Bách Khoa – Takenaka đã làm lễ khởi công Nhà máy sản xuất Hormone – Steroid – Thuốc dùng ngoài theo tiêu chuẩn EU-GMP và PIC/S tại Khu công nghiệp VSIP (Bình Dương). Sau khi hoàn thành, Phân xưởng này sẽ là nhà máy sản xuất dược phẩm hormone và steroid đầu tiên tại Việt Nam và là một trong số ít nhà máy của ASEAN được xây dựng theo tiêu chuẩn Châu Âu với nhà xưởng, tiện ích, máy móc trang bị và quy trình công nghệ hiện đại.
Được biết, thuốc Molnupiravir Stella 400 mg, do Công ty TNHH Liên doanh Stellapharm - chi nhánh 1, giá bán 12.500 đồng/viên. Một hộp thuốc Molnupiravir đóng gói 20 viên 400 mg hoặc 40 viên 200 mg đủ cho một liệu trình điều trị. Như vậy, giá thuốc dao động từ 230.000 đến dưới 350.000 một hộp cho liệu trình 5 ngày.
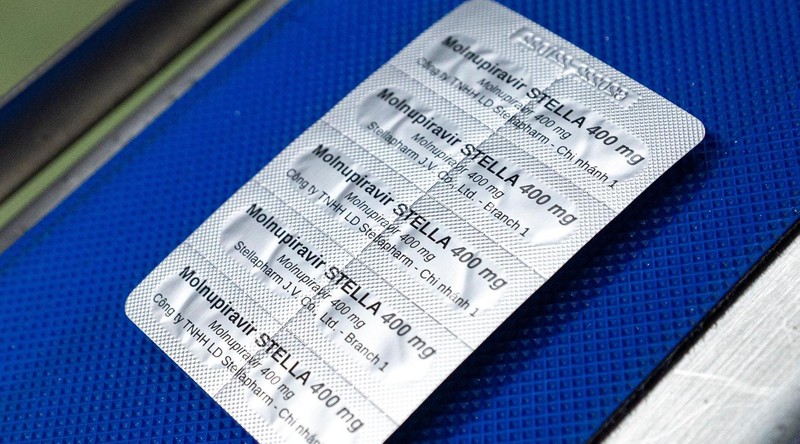 |
Monulpiravir Stella 400g - Ảnh: Tiền Phong |
Kỳ vọng lớn về thuốc tốt giá rẻ cho người Việt
Thuốc Molravir 400 dạng viên nang cứng do Công ty Cổ phần Dược phẩm Boston Việt Nam (số 43, đường số 8, KCN Việt Nam – Singapore, phường Bình Hoà, TP. Thuận An, tỉnh Bình Dương) đăng ký và sản xuất.
Từ những ngày đầu tiên được thành lập, BOSTON PHARMA lấy tên là Công ty Cổ phần Dược Phẩm VITAR do Tổng công ty Dược Việt Nam (Đại diện là Công ty dược Trung ương I) và các cổ đông cá nhân có kinh nghiệm trong ngành dược phẩm điều hành.
Với những điểm chung về tầm nhìn, sứ mệnh, Công ty đã quyết định hợp tác cùng với Boston Pharmaceutical Inc USA để cùng cộng hưởng phát triển và hướng đến chăm sóc sức khỏe cho cộng đồng.
Năm 2008, Công ty Cổ phần Dược phẩm Boston Việt Nam (gọi tắt là BOSTON PHARMA) chính thức đổi tên theo sự liên doanh và nhượng quyền từ Boston Hoa Kỳ.
 |
| Cận cảnh quy trình sản xuất thuốc điều trị COVID-19. Ảnh: Tiền Phong |
Đơn vị cuối cùng được cấp phép sản xuất thuốc đặc trị COVID-19 được thành lập từ năm 1975, với tên gọi là Xí nghiệp Dược phẩm Trung ương 24, là đơn vị thành viên của Tổng công ty Dược Việt Nam.
Đến năm 1985 Xí nghiệp sáp nhập với Xí nghiệp dược phẩm Trung ương 22, đổi tên thành Xí nghiệp dược phẩm Trung ương 24 – MEKOPHAR.
Năm 1993, Xí nghiệp liên doanh với Công ty Woopyung - Hàn Quốc thành lập Công ty liên doanh Woopyung - Mekophar, sản xuất nguyên liệu kháng sinh bán tổng hợp như: Amoxicilin, Ampicilin.
Năm 2000, Xí nghiệp dược phẩm Trung ương 24 mua lại toàn bộ phần vốn của đối tác liên doanh và Công ty liên doanh Woopyung-Mekophar trở thành phân xưởng sản xuất Kháng sinh Bêta lactam của Xí nghiệp dược phẩm Trung ương 24.
Năm 2001, Công ty chính thức đổi tên thành Công ty Cổ phần Hoá - Dược phẩm Mekophar. (Theo Quyết định số 1589/QĐ-TTg, ngày 19/12/2001 của Thủ tướng Chính phủ về việc chuyển Xí nghiệp Dược phẩm Trung ương 24 - đơn vị trực thuộc Tổng Công ty Dược Việt Nam thành Công ty cổ phần). Chính thức chuyển đổi sang hoạt động theo mô hình công ty cổ phần, với vốn điều lệ ban đầu là 36 tỷ VNĐ.
Năm 2003, Công ty đã góp vốn thành lập Bệnh viện đa khoa An Sinh và Bệnh viện đã đi vào hoạt động ngày 07/05/2006.
Năm 2006, Công ty phát hành cổ phiếu lần đầu (IPO) ra công chúng. Mã chứng khoán MKP, tăng vốn điều lệ lên 84 tỷ VNĐ.
Năm 2008, thành lập Ngân hàng tế bào gốc MekoStem (theo quyết định số 4001/UBND-VX do UBND Tp.Hồ Chí Minh ban hành ngày 25/06/2008) và được Bộ Y tế cấp giấy phép hoạt động (số 3144/QĐ-BYT) ngày 30/08/2011. Vốn điều lệ được tăng lên 92,1 tỷ VNĐ.
Năm 2010, Công ty niêm yết cổ phiếu và giao dịch trên sàn HOSE (Sở Giao dịch Chứng khoán TP. Hồ Chí Minh). Năm 2011, tăng vốn điều lệ lên: 101.159.320.000 VNĐ. Năm 2014, tăng vốn điều lệ lên: 131.234.130.000 VNĐ. Năm 2015, tăng vốn điều lệ lên: 151.234.130.000 VNĐ. Năm 2016, tăng vốn điều lệ lên: 194.208.130.000 VNĐ.
Mới đây, Bộ Y tế đã công khai giá bán ba loại thuốc Molnupiravir do Việt Nam sản xuất, loại thấp nhất giá 8.675 đồng/viên, cao nhất 12.500 đồng/viên.
Trong giai đoạn dịch COVID-19 đang bùng phát mạnh như hiện tại ở Hà Nội và nhiều tỉnh thành trên cả nước, việc ba đơn vị được cấp phép sản xuất thuốc đặc trị Molnupiravir tại Việt Nam đã nhen nhóm lên niềm hy vọng về việc sản xuất thuốc tốt giá rẻ cho người Việt.
3 loại thuốc điều trị COVID-19 được Bộ Y tế cấp phép sản xuất trong nước

Giai đoạn bùng dịch mới, biến chủng Omicron “oanh tạc” TP.HCM