Được biết, cơ quan Khoa học y tế Singapore (HSA), Cơ quan quản lý dược phẩm Thụy Sĩ (Swissmedic) đã có thông báo về việc thu hồi các thuốc chứa Ranitidine do phát hiện các thuốc này chứa tạp chất N-nitrosodimethylamine (NDMA) có nguy cơ gây ung thư ở hàm lượng vượt quá ngưỡng cho phép của quốc tế.
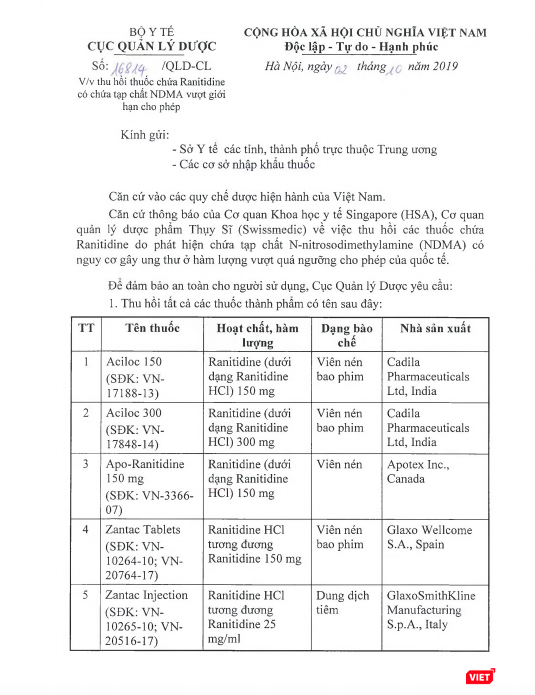
Để đảm bảo an toàn cho người sử dụng, Cục Quản lý Dược yêu cầu thu hồi tổng cộng 11 thuốc thành phẩm chứa Ranitidine.
 |
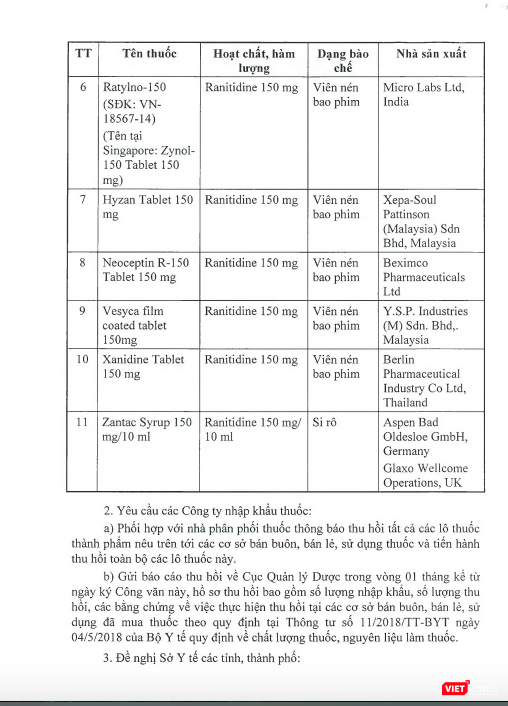 |
Cục Quản lý Dược yêu cầu các Công ty nhập khẩu thuốc phối hợp với nhà phân phối thuốc thông báo thu hồi tất cả các lô thuốc thành phẩm nêu trên tới các cơ sở bán buôn, bán lẻ, sử dụng thuốc và tiến hành thu hồi toàn bộ các lô thuốc này. Gửi báo cáo thu hồi về Cục Quản lý Dược trong vòng 1 tháng kể từ ngày ký Công văn.
Hồ sơ thu hồi bao gồm: số lượng nhập khẩu, số lượng thu hồi, các bằng chứng về việc thực hiện thu hồi tại các cơ sở bán buôn, bán lẻ, sử dụng đã mua thuốc theo quy định của Bộ Y tế về chất lượng thuốc và nguyên liệu làm thuốc.
Cục Quản lý Dược cũng đề nghị Sở Y tế các tỉnh, thành phố thông báo việc thu hồi tới các cơ sở kinh doanh, sử dụng thuốc trên địa bàn, đồng thời, công bố thông tin việc thu hồi tất cả các thuốc thành phẩm nêu trên trên Trang thông tin điện tử của Sở. Từ đó, kiểm tra và giám sát các Công ty nhập khẩu thuốc trên địa bàn thực hiện việc thu hồi thuốc.